拝啓 時下ますますご清栄のこととお慶び申し上げます。
2021年8月1日より、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下「薬機法」)の改正によって、体外診断用医薬品、医療機器の添付文書が電子化されることになりました。
体外診断用医薬品、医療機器の添付文書を閲覧する場合は、スマートフォン等の専用アプリケーション(添付文書閲覧アプリ。以下、添文ナビ)を用い、製品の外箱等に印字されたGS1 バーコードを読み取ることで、独立行政法人医薬品医療機器総合機構のホームページ上に掲載されている電子化された添付文書(以下、電子添文)や関連文書をご確認いただくことになります。
以下、今後の添付文書同梱廃止に関する予定、電子添文の閲覧方法、初回納品時および電子添文改定時の対応についてご案内申し上げます。
1. 貴社にご購入いただいている製品の添付文書同梱廃止時期について
2023年7月31日以降紙媒体の添付文書の同梱を終了いたします。
2. 電子添文の閲覧方法について
1) 添文ナビを利用して閲覧する方法
弊社が製造販売している製品の外箱に、GS1バーコードを表示しています。
その表示を専用アプリケーション(添文ナビ)で読み取ることで、電子添文を閲覧いただけます。 (使用方法は4.をご参照ください)
2) PMDAのホームページより閲覧する方法
PMDAのホームページにも同じ電子添文が掲載されておりますので、そちらでも閲
覧可能です。
3. 初回納品時の情報提供
同梱を廃止した製品については、添文ナビの利用による電子添文またはPMDAホーム
ページ掲載の電子添文をもって、情報提供とさせていただきます。
なお、紙媒体での提供をご要望される場合は、弊社営業担当者にお申し付けください。
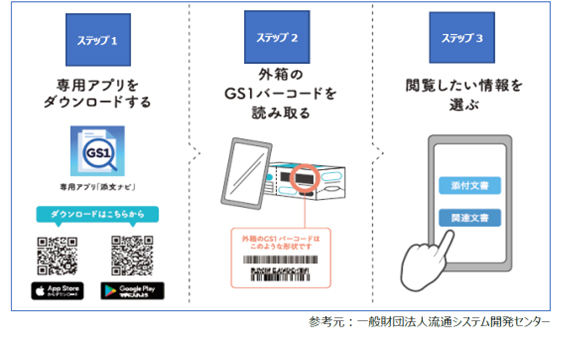
4. 添文ナビによる電子添文の閲覧方法
関連通知
■令和 3年 2月 19日付 薬生安発 0219 第1号
厚生労働省医薬・生活衛生局医薬安全対策課長通知
「医薬品等の注意事項等情報の提供について」
■令和 3年 2月 19日付 6月 11日一部改正、7月14日一部改正)
厚生労働省医薬・生活衛生局医薬安全対策課事務連絡
「医薬品等の注意事項等情報の提供について」に関する質疑応答集(Q A)について
関連サイト
■PMDA(独立行政法人 医薬品医療機器総合機構) 「添付文書の電子化について」
https://www.pmda.go.jp/safety/info-services/0003.html
■一般財団法人流通システム開発センター(GS1 Japan) 添付文書閲覧アプリ「添文ナビ」
https://www.dsri.jp/standard/healthcare/tenbunnavi/app/index.html
以上
